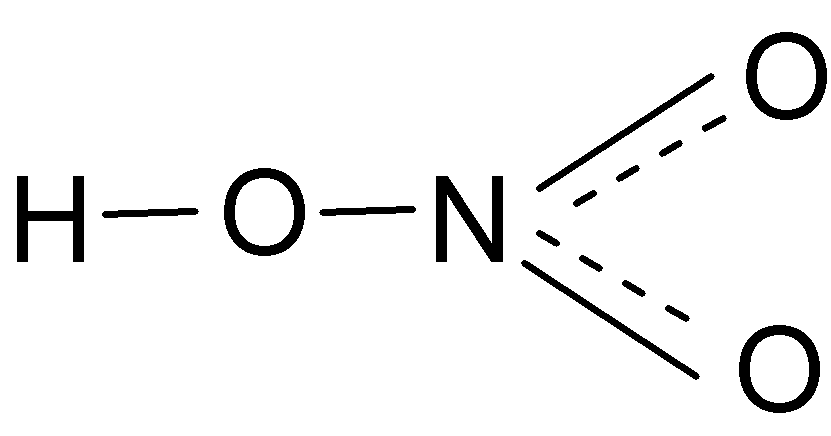
Азотная кислота (
HNO3) - сильная одноосновная кислота; безводная азотная кислота - бесцветная жидкость, слабо дымящаяся на воздухе; удельный вес = 1,59 (при 15 °C), температура кипения 86 °C; на свету и при нагревании желтеет в результате образования диоксида азота (
NO2).
Свойства азотной кислоты:
Характерным свойством азотной кислоты является ее ярко выраженная окислительная способность.
Азотная кислота - один из энергичнейших окислителей. Азотная кислота действует почти на все металлы (кроме благородных, платины, тантала, родия, иридия), превращая их в нитраты, а некоторые металлы в оксиды.
Азотная кислота сильно действует на ткани организма не только водородными ионами, но и анионами, разлагая белок. При этом в местах контакта кислоты с кожей или слизистыми оболочками происходит ксантопротеиновая реакция (возникает жёлтое окрашивание).
Получение азотной кислоты:
Азотную кислоту получают контактным способом путём окисления аммиака воздухом на платиновом катализаторе (по методу Оствальд–Кульмана) или из селитры отгонкой с серной кислотой.
Дымящую азотную кислоту получают пропусканием диоксида азота сквозь концентрированную азотную кислоту или перегонкой при повышенной температуре селитры с серной кислотой.
Меры предосторожности:
При отравлении азотной кислотой возникает резкая жгучая боль в пищеводе, желудке; рвота, иногда судороги; бледность, пот, пульс частый, слабый, аритмия, анурия.
Рвота при отравлении азотной кислотой сопровождается кашлем и затруднением дыхания вследствие отёка гортани.
Смертельная доза концентрированной азотной кислоты: 8–10 мл.
Препараты азотной кислоты:
Кислота азотная очищенная
Содержит 32,4 % безводной
HNO3, применяется для прижиганий.
Кислота азотная разведенная
Содержит 16,2 % безводной азотной кислоты.
Кислота азотная дымящая
86 % азотная кислота содержащая до 8 %
NO2, обильно выделяет удушливые пары диоксида азота.
Историческая справка:
Азотная кислота впервые получена Гебером в VIII веке.
Состав азотной кислоты определён Гей-Люссаком в 1816 году.
Применение азотной кислоты:
- приготовление азотнокислого серебра (ляписа, адского камня), употребляемого в фармацевтическом и фотографическом деле;
- с помощью азотной кислоты готовится хлопчатобумажный порох, пикриновая кислота, фталевая кислота, ализарин, гремучее серебро;
- в производстве минеральных удобрений;
- в военной промышленности (дымящая — в производстве взрывчатых веществ, как окислитель ракетного топлива, разбавленная — в синтезе различных веществ, в том числе отравляющих);
- в станковой графике — для травления печатных форм (офортных досок, цинкографических типографских форм и магниевых клише).
- в производстве красителей и лекарств (нитроглицерин)
- в ювелирном деле — основной способ определения золота в золотом сплаве.
Чтобы купить азотную кислоту воспользуйтесь формой ниже, введя нужное количество литров и нажмите на клавишу «положить в корзину».
 Химическая продукция
Химическая продукция
 Ищете, где купить азотную кислоту в Перми, Уфе, Екатеринбурге, Красноярске, или Хабаровске?
Ищете, где купить азотную кислоту в Перми, Уфе, Екатеринбурге, Красноярске, или Хабаровске?
